Introducción
Una de las etapas más importantes utilizada en el refino de petróleo es el proceso de craqueo catalítico en lecho fluidizado. La principal característica de este proceso es la conversión de fracciones pesadas del petróleo en productos más ligeros y, consecuentemente, con mayor valor agregado.
Son utilizados catalizadores zeolíticos para promover las reacciones de quiebra de moléculas, siendo un ejemplo de catálisis heterogénea. La zeolita del tipo Y es la principal zeolita utilizada para el craqueo catalítico de fracciones del petróleo. Esta posee propiedades tales como: estructura cristalina y tamaño de poros bien definidos, elevada área específica y alto grado de acidez. Inicialmente esta zeolita es sintetizada bajo la forma de NaY, la cual no posee actividad catalítica ácida. Por lo tanto, se hace necesario el proceso de intercambio iónico, donde los cationes Na+ son sustituidos por NH4+. El catión H+, que es el responsable por la actividad catalítica de la zeolita, es fijado a la estructura después del proceso de calcinación de la zeolita, en el cual el ion amonio se descompone en amonio y H+.
Una de las configuraciones utilizadas en larga escala para el intercambio iónico de la zeolita NaY es la de reactores tanques de mezcla seguidos de un sistema en lecho fijo. En este último, la zeolita es colocada en un sistema de filtración del tipo estera a vacío, y después de la formación de una torta con cierta porosidad, el sistema es alimentado con líquidos de intercambio iónico, normalmente soluciones acuosas de cloruro de amonio y cloruro de tierras raras. Los líquidos filtran la torta y, a través de la transferencia de masa difusional en los poros, las especies químicas de interés son intercambiadas, removiendo las especies químicas indeseables, que en el caso de la NaY son los cationes Na+. A través de la aplicación de vacío, se remueve el filtrado, y la zeolita intercambiada, permanece bajo la forma de torta.
Sistemas de adsorción seguidos de intercambio iónico pueden tener su comportamiento global representado por curva de ruptura. Esta muestra la saturación progresiva de un lecho fijo por el adsorbato utilizado. Modelos matemáticos son utilizados para describir la curva de ruptura, debido a la dinámica de columnas de intercambio iónico. A través de la utilización de modelos, optimizaciones en el proceso en escala industrial pueden ser realizadas, tales como: disminución del consumo de las materias primas y aumento de la producción. La evaluación de los modelos fue el principal objetivo de este trabajo, y la validación de los modelos puede ser realizada por medio de levantamiento de datos en escala de laboratorio, preferencialmente en condiciones semejantes a las utilizadas en plantas industriales.
Así, fue evaluado el efecto de la altura del lecho de zeolita durante el intercambio iónico en columna de lecho fijo, utilizando la zeolita NaY parcialmente intercambiada (NaNH4Y) en reactores tanques de mezcla. Basado en la literatura, el presente trabajo fue desarrollado en las siguientes etapas: levantamiento de las isotermas de adsorción, obtención de las curvas de ruptura en condiciones similares a las del proceso industrial y comparación entre las previsiones de los modelos y los datos.
Experimental
Pre Tratamiento de la Zeolita Y Parcialmente intercambiada
La zeolita utilizada en el presente trabajo fue cedida por Fábrica Carioca de Catalisadores S.A. (FCCSA). Se trata de una zeolita del tipo Y oriunda del proceso de intercambio iónico parcial realizado en reactores de mezcla, representando una disminución de 40 % en su capacidad disponible de intercambio, o sea, aproximadamente 28 % de la capacidad total. En este trabajo representaremos tal zeolita por NaNH4Y. Inicialmente la zeolita NaNH4Y fue lavada con agua destilada para remoción de iones amonios residuales de la primera etapa de intercambio iónico. El sólido recogido fue llevado a la estufa a 105 °C durante 30 minutos para secado.
Caracterización de la Zeolita NaNH4Y
La composición química de la NaNH4Y fue determinada por fluorescencia de rayos X, utilizando un aparato FRX Axios de Panalytical, operando a 50 kV y 125 mA. Para la determinación de las propiedades texturales, las muestras en polvo fueron pre tratadas a vacío (6,7 Pa), a 300 °C por 1 h y fue utilizado el método de adsorción de nitrógeno a -195,8 °C, en equipamiento TRISTAR II Micromeritics. La distribución de tamaños de partículas fue obtenida en difractómetro a laser de la marca Malvern, modelo Mastersizer 2000, que caracteriza las partículas por el diámetro de la esfera del mismo volumen que ellas.
Equilibrio de Intercambio Iónico
La adsorción, que es una etapa intermediaria del proceso de intercambio iónico, fue estudiada a través de las llamadas isotermas de adsorción. El método de inmersión en volumen finito, más conocido como baño finito, fue utilizado para obtener las concentraciones de equilibrio. Los ensayos fueron realizados en baño termostático (40 °C), usando el equipamiento IKA®TS2 TEMPERIERBAD.
El procedimiento experimental consistió en secar y pesar la zeolita NaNH4Y y suspenderla en la solución de NH4Cl, preparada a partir del cloruro de amonio P.A con 99,8% de pureza. Las isotermas de adsorción fueron realizadas en las concentraciones de 150, 300, 400, 600, 900, 1.200 y 1.600 ppm de amonio, donde el pH de las soluciones fueron corregidos para 4,5 con ácido clorhídrico P.A. Todas las soluciones, preparadas en diferentes concentraciones, fueron analizadas en espectrofotómetro Spectroquant® NOVA 60 (Merck) para confirmar la concentración de amonio deseada.
Las alícuotas para análisis espectrofotométrica fueron retiradas 18 horas después del inicio del experimento. Ensayos preliminares mostraron que un tiempo en torno a 18 horas era suficiente para alcanzar el equilibrio de intercambio iónico.
Curvas de Ruptura
Los ensayos en columna de lecho fijo de zeolita NaNH4Y buscaron determinar su capacidad de intercambio iónico así como evaluar el efecto de la altura del lecho sobre el proceso. La unidad de laboratorio utilizada para levantamiento de las curvas de ruptura se muestra esquemáticamente en la Figura 1.

La solución de cloruro de amonio fue alimentada a la columna, con flujo descendiente y flujo de aproximadamente 1 mL min-1, por medio de una bomba peristáltica. La columna utilizada fue una bureta graduada, de 50 cm de largo y 1,1 cm de diámetro interno. Fue fijado en la columna, por medio de anillo del tipo o’ring, un medio filtrante de polipropileno cuyo objetivo era soportar el lecho de zeolita. Muestreos eran realizados en la salida de la columna, en intervalos conocidos, para determinación de la concentración de amonio hasta que la saturación de la zeolita fuese conseguida y la solución en la salida de la columna alcanzase la concentración de la alimentación.
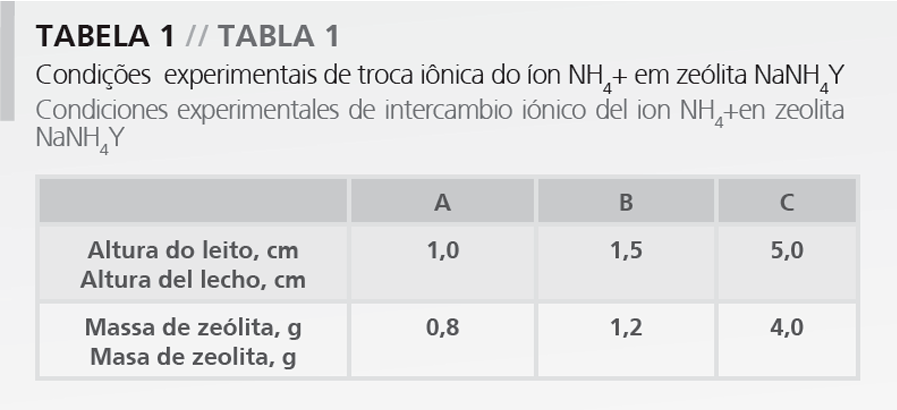
Con el fin de evaluar los efectos de la altura de la columna en el intercambio iónico en lecho fijo, fueron realizados ensayos a 40°C con soluciones de cloruro de amonio con concentración de 300 ppm de amonio, flujo de 1 mL min-1 y pH 4,5. Las condiciones operacionales en cada ensayo son mostradas en la Tabla 1.
Resultados y Discusión
Caracterización de la ZeolitaNaNH4Y
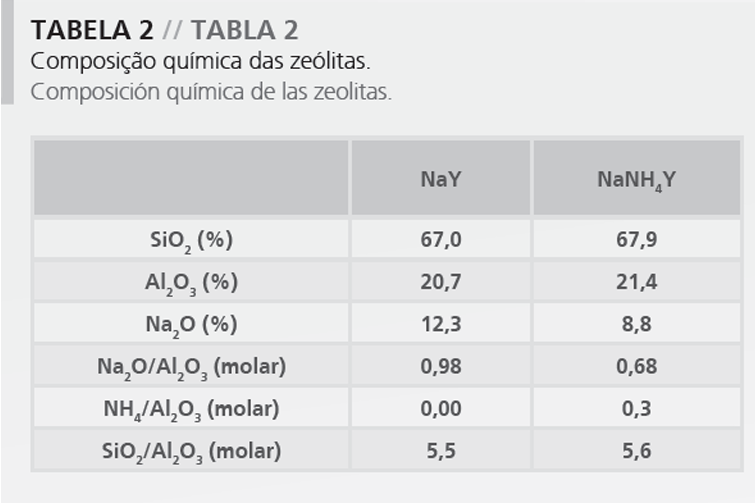
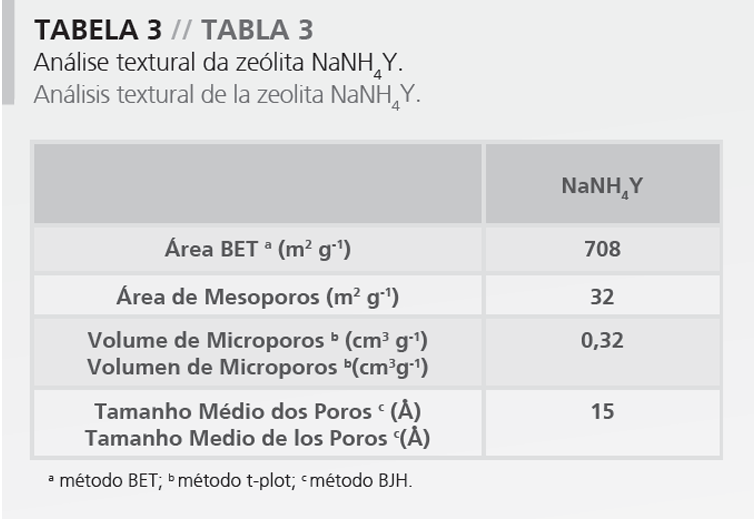
La composición química de las zeolitas NaY (no intercambiada) y NaNH4Y (parcialmente intercambiada) está presentada en la Tabla 2. Las propiedades texturales son presentadas en la Tabla 3. Los porcentajes acumulativos para tres tamaños de partículas de la zeolita NaNH4Y son presentados en la Tabla 4.

Equilibrio de Intercambio Iónico
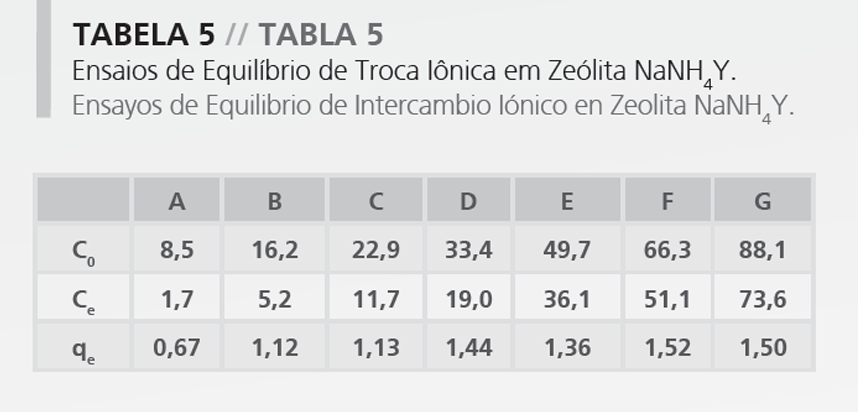
Las condiciones experimentales de los ensayos de equilibrio de intercambio iónico están descritas en la Tabla 5, y la concentración de equilibrio en sólido fue calculada a través de la Ecuación 1:
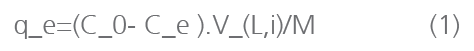
Donde, qe (mmol g-1) es la concentración de amonio en la fase sólida, en el equilibrio, Ce(mmol L-1) es la concentración de amonio en la fase líquida, en el equilibrio, C0(mmolL-1) es la concentración inicial de amonio en la fase líquida, VL,i (L) es el volumen inicial de líquido y M (g) es la masa de zeolita.
La Figura 2 presenta los datos de concentraciones del ion amonio en equilibrio en la fase sólida (qe) y en la fase líquida (Ce) a 40 °C, y los ajustes de las isotermas de Langmuir y Freundlich.

Los modelos de Langmuir y Freundlich fueron escogidos para representar el equilibrio del sistema estudiado. El modelo de Langmuir ajustó mejor los datos experimentales y la capacidad máxima de intercambio iónico obtenido fue 1,52 mmol g-1, lo que equivale a 27,5 mgg-1.
Curvas de Ruptura
La Figura 3 muestra el efecto de la altura del lecho bajo las curvas de ruptura utilizando una concentración de alimentación de 300 ppm de NH4+ y flujos prácticamente constantes (1,0 mL min-1). Cabe resaltar que bajo vacío la altura del lecho no varió con el tiempo.

Conforme esperado, mayores tiempos de ruptura y saturación fueron obtenidos a medida que aumentó la altura del lecho de zeolita. Lechos más altos demoraron más tiempo para alcanzar la saturación.
Modelos de Curva de Ruptura
Los modelos de curva de ruptura fueron evaluados basados en los datos obtenidos. La Tabla 6 muestra resumidamente las ecuaciones de los modelos matemáticos que fueron abordados en este trabajo.
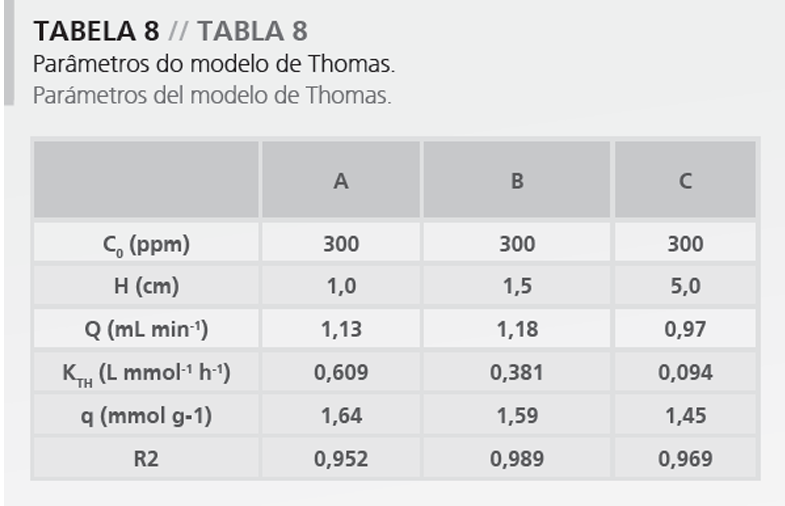
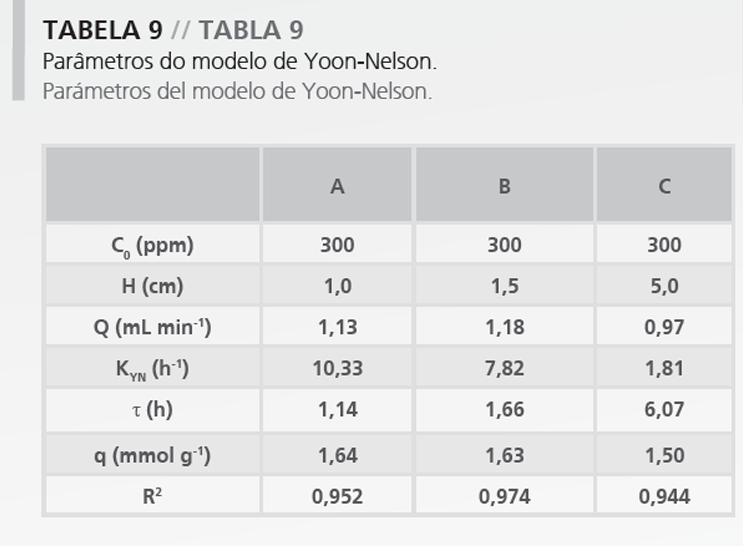
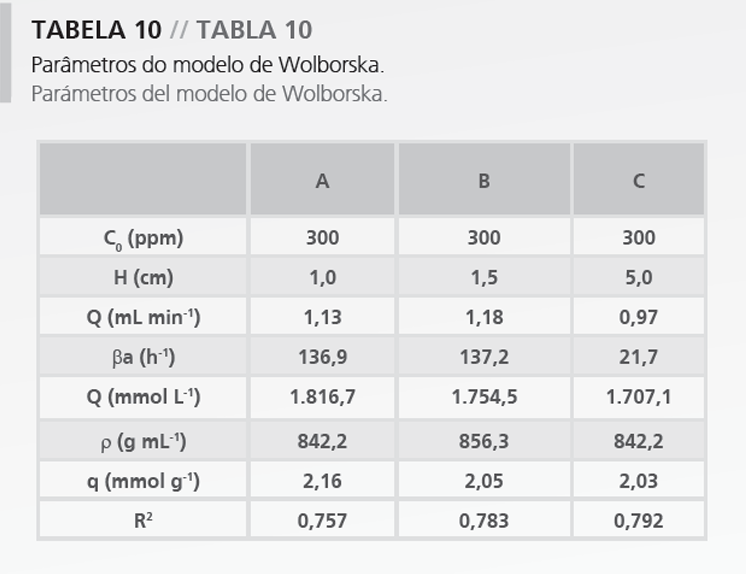
A partir de las curvas de ruptura experimentales y de las formas linealizadas de los referidos modelos, fueron determinados sus parámetros. En las Tablas 7 a 10 están presentados los parámetros obtenidos en el ajuste de los modelos de Bohart-Adams, Thomas, Yoon-Nelson y Wolborska, respectivamente, y sus coeficientes de determinación (R2).


La constante cinética del modelo de Bohart-Adams (KBA) decrece con el aumento de la altura del lecho. No hubo diferencia significativa en los valores de capacidad de intercambio iónico cuyo valor medio fue 1,56 mmolg-1.
Hubo una disminución para los valores de la constante de velocidad del modelo de Thomas (KTH) con el aumento de la altura del lecho. Estudios similares al evaluar el intercambio iónico en zeolita, obtuvieron comportamientos semejantes. Las capacidades de intercambio iónico (q) quedaron entre 1,45 a 1,64 mmolg-1, un rango relativamente estrecho de valores. Fueron obtenidos coeficientes buenos de determinación, entre 0,95 y 0,99. Los modelos de Bohart-Adams y Thomas son matemáticamente equivalentes. Eso explica la semejanza de los valores de los parámetros KBA eKTH así como los valores de q.
Según el modelo de Yoon-Nelson, cuanto mayor es la altura del lecho menor es el valor de KYN. Otro parámetro importante determinado por el modelo de Yoon-Nelson es el t tiempo en el cual C/C0 » 0,5. Cuanto mayor es la altura del lecho mayor fue el valor de t. Las capacidades de intercambio iónico quedaron entre 1,50 a 1,64 mmolg-1. Los coeficientes de determinación tuvieron valor medio de 0,96.
Los coeficientes de determinación muestran que el modelo de Wolborska no ajustó los datos. Una de las posibles causas puede estar relacionada a la existencia de dispersión axial de masa asociada a los altos valores del parámetro ba. De acuerdo con la literatura, el modelo es adecuado apenas para valores de C/C0< 0,5.
Con los parámetros calculados de los modelos, fueron generadas las curvas de ruptura para cada modelo y comparadas a las curvas experimentales. La Figura 4 presenta las curvas de ruptura obtenidas por los modelos para alturas de lecho de 1,0, 1,5 y 5,0 cm, respectivamente.
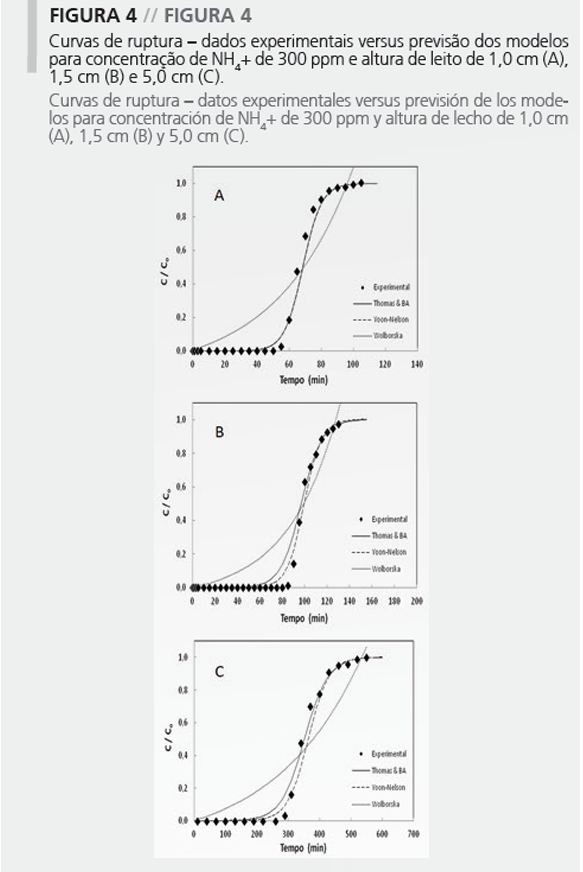
La Tabla 11 compara los tiempos de saturación obtenidos experimentalmente con los previstos por los modelos de Bohart-Adams, Thomas, Yoon-Nelson y Wolborska para C/C0 = 0,99.

Los modelos de Thomas y Bohart-Adams mostraron un desvío medio en relación a los datos de 3,2%, mientras los de Yoon-Nelson y Wolborska fueron de 4,1% y 3,8%, respectivamente. Conforme esperado, los menores tiempos de saturación fueron en las menores alturas de lecho.
La capacidad de intercambio iónico del lecho de zeolita pudo ser obtenida a través del balanceo de masa de NH4+en la columna, a partir do monitoreo de la concentración de salida en función del tiempo. Para efectuar este cálculo es necesario garantizar que la columna esté saturada, es decir, la concentración en la salida de la columna debe ser igual a la concentración de alimentación.
La capacidad de intercambio iónico de la columna es dada por la Ecuación 2:
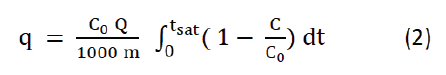
Donde, q es la concentración de equilibrio de los iones amonio en la zeolita (mmolg-1), m es la masa seca de zeolita (g), Q es el flujo volumétrico de la solución (mLmin-1), tsat es el tiempo de saturación en minutos, C es la concentración de amonio en la salida de la columna (mmol L-1) y C0 es la concentración de amonio en la alimentación de la columna (mmol L-1).
La Tabla 12 presenta las capacidades de intercambio iónico (q) de los experimentos y las previstas por los modelos para C/C0 = 0,99. Debido al ajuste malo del modelo de Wolborska, el mismo no tuvo su capacidad de intercambio comparada a los demás.

Las capacidades de intercambio obtenidas por los modelos quedaron próximas de las experimentales, calculadas a través de la Ecuación2. Mientras los modelos de Thomas y Bohart-Adams resultaron en un desvío medio de 2,4% en relación a los datos, el desvío medio para el modelo de Yoon-Nelson fue de 1,4%. La capacidad de intercambio de la columna expresa en mmolg-1, resultó, en principio, a valores muy próximos para todos los experimentos. El valor medio fue de 1,58 mmolg-1, que quedó próximo de la capacidad máxima de intercambio (qm) obtenida en los ensayos de equilibrio de intercambio iónico (1,52 mmolg-1).
La capacidad de intercambio catiónico (CTC) de la zeolita NaY es 3,90 meq g-1, donde la composición molar de la cela unitaria en base seca es Na51. [(AlO2)51.(SiO2)141]. Por lo tanto, fue posible comparar los valores de CTC experimentales y de los modelos con el teórico. Según la literatura, 32% de iones Na+ no pueden ser sustituidos en la zeolita Y cuya razón molar sílice-alúmina (SAR) es de 5,6. Conforme ya citado, cerca de 40% del Na+ disponible para el intercambio en la zeolita NaY fue intercambiado en reactores de mezcla, a montante del punto donde fueron obtenidas las muestras de zeolita, designada en este trabajo por NaNH4Y. Así, la capacidad de intercambio de la zeolita utilizada es de 3,9 x (1 - 0,32) x 0,6 = 1,59 mmolg-1, próxima de las obtenidas en los experimentos y de las previstas por los modelos.
Conclusiones
Los modelos de Bohart-Adams, Thomas y Yoon-Nelson se mostraron los más adecuados arepresentación de la curva de ruptura en el intercambio iónico de la zeolita NaNH4Y. El modelo de Wolborska no se ajustó a los datos, lo que es explicado en términos de los altos valores de C/C0 utilizados en este trabajo. Los modelos de Bohart-Adams y Thomas son matemáticamente equivalentes y, por esa razón generaron curvas de ruptura superpuestas. Las curvas de ruptura mostraron que cuanto mayor es la altura del lecho, mayores son los tiempos de ruptura y saturación. Los datos de equilibrio de intercambio iónico obtenidos fueron bien descritos por la isoterma de Langmuir. Para los experimentos en lecho fijo, las capacidades medias de intercambio de Na+ por NH4+ fueron de 1,61, 1,64 y 1,48 mmolg-1 para alturas de lecho de 1,0, 1,5 y 5,0 cm, respectivamente. Estos valores además de estar próximos a la capacidad de intercambio obtenida en el levantamiento de las isotermas corroboran que 28% del intercambio iónico de la zeolita utilizada ya había sido realizado.
-

- de
-


































¿Qué le pareció la publicación?